近日,中央政治局会议首提“反内卷”,引发市场热议。随后“强化行业自律,防止‘内卷式’恶性竞争”的话题也登上医药产业新闻的头条。
实际上,国内创新药产业如肿瘤靶点方面的“内卷”由来已久。如今在政策明确导向下,对创新药企提出的新课题已经不是“有没有”的问题,而是“优不优”的问题。只有如一品红这类创新药企,把资源集中起来,在某一领域做深做透,做出差异化,或许能走出一条破“卷”之道。
以一品红最新获批临床的口服小分子GLP-1R激动剂为例,据公告披露,APH01727片是一品红药业自主研发的一款高活性高选择性的胰高血糖素样肽-1受体激动剂(GLP-1RA),目标成为每天给药一次的口服小分子GLP-1R激动剂,拟用于2型糖尿病、超重/肥胖患者的治疗。
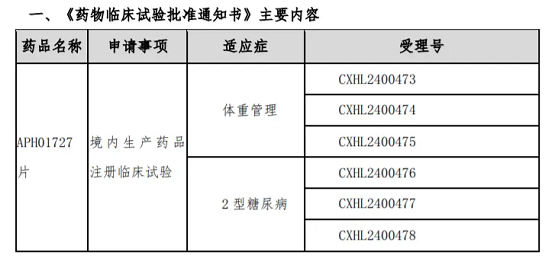
虽然目前全球GLP-1药物研发火热且不乏有诺和诺德司美格鲁肽这种爆款存在,但实际上,APH01727所在的口服小分子GLP-1R激动剂赛道,目前尚无产品在国内外批准上市。业内观点认为,与大分子GLP-1RA相比,口服小分子GLP-1RA优势明显:分子量小,可避免皮下注射,且服药不受饮食和剂量的限制,大大提高了患者的服药依从性。
除了通过产品和剂型创新在热门靶点“反内卷”外,不同于目前多数扎堆于免疫检查点抑制剂开发以及主打肿瘤适应症治疗的创新药企,一品红还颇具特色地选择痛风领域作为其创新管线战略聚焦的主赛道。
从市场临床价值导向的角度来看,全球范围内,生物药在痛风领域还处于开拓阶段。当前全球痛风病发病率呈增高趋势且治疗痛风需要长期用药,然而现有治疗方式及药物如别嘌醇、非布司他等疗效有限且存在较大的用药安全隐患,因而市场对新型安全的治疗药物存在较大的未满足临床需求。
目前URAT1抑制剂国内仅苯溴马隆获批上市,多替诺雷于今年1月22日申报上市;在研方面,目前国内处在研发第一梯队的有恒瑞医药、璎黎药业、先声药业、信诺维和一品红等企业。
但AR882此前已完成的全球多中心IIb临床试验数据显示:与现有疗法相比,AR882治疗痛风患者的疗效更显著,安全性更高。AR882除了能降低痛风患者的sUA水平,还能显著减少痛风石、减轻尿酸结晶负担及降低痛风急性发作率,产品的best-In-Class潜质更为凸显。
AR882作为一款真正具备重大创新性的药物,其降低尿酸、溶解痛风石的临床成果获得美国FDA高度认可,先后在2023年美国风湿病学会(ACR)年会和2024欧洲风湿病学大会(EULAR)年会上亮相,赢得了国际医学界的广泛赞誉。目前,该项目已进入全球多中心III期临床试验。
按照计划,今年6月,AR882迎来了其研发历程中的一个重要里程碑——全球关键性的Ⅲ期临床研究REDUCE 2试验成功完成了首例患者给药。随着这一关键进展的实现,AR882的临床研究已经进入了一个新的阶段。此次REDUCE 2试验将与今年下半年启动的验证性研究REDUCE 1同步展开,为AR882的疗效和安全性提供更为全面和深入的科学证据。
从市场前景来看,仅以国内为例,据FRost&Sullivan预测,我国高尿酸血症及痛风患病人数会在2030年达到2.4亿人,而国内痛风药物市场规模将从2016年的9亿元增长至2020年的28亿元,并预计于2030年增长至108亿元。这显然有望为一品红后续进一步打开增长空间。
值得一提的是,战略聚焦痛风领域并不意味着一品红将放弃其他项目,而是通过重点推进方式助推管线中重磅项目的运作和推进。除了上述提到的口服小分子GLP-1R激动剂外,今年6月份,一品红研制的针对高血压人群的坦络定®奥美沙坦酯口崩片通过一致性评价。
该药是ARB(血管紧张素Ⅱ受体拮抗剂)类首家国内上市的口腔崩解剂,该药不仅具有降压作用,还可保护心脏和肾脏功能,改善高血压对心脑肾等靶器官的损害,降低心脑血管事件发生风险。在原研药未进入国内销售的市场背景下,该药的上市将极大满足国内庞大的未满足治疗需求。
一品红在创新药领域的潜在增长空间也被国内一众券商看好。西部证券在近期首次覆盖一品红的研报中表示公司“存量品种稳健增长,痛风新药打开长期空间”,并予以了“买入”评级;华安证券和华泰证券则分别表示公司“AR882研发取得阶段性成果,全球化创新再启新程”、“AR882再证BIC潜力”,并同样予以公司“买入”评级。